1.化学反应原理![]()
如图5-1所示,利用磷燃烧消耗空气中的氧气,从而使容器内形成负压,打开止水夹后,水进入容器内。进入容器中的水的体积,可粗略地认为是空气中所含氧气的体积。![]()
![]()
![]()
![]()
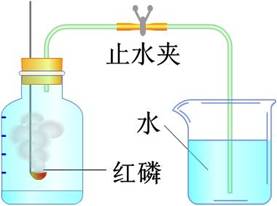 图5-1
图5-1![]()
2.实验仪器:集气瓶、燃烧匙、烧杯、玻璃管、乳胶管、止水夹。![]()
实验药品:红磷、水。![]()
3.探究方案:![]()
⑴ 在集气瓶中放入少是水(用于溶解生成的五氧化二磷,同时可吸收燃烧产生的热,有利于瓶内降温),做上记号,并将瓶内剩余体积均分为五等分。![]()
⑶ 用止水夹夹紧乳胶管,点燃燃烧匙内的红磷后,立即伸入集气瓶中并把塞子塞紧。观察到红磷燃烧,产生浓厚的白烟。![]()
⑶红磷熄灭后,冷却至室温,打开止不夹,观察到水进入集气瓶内,最终水面在五分之一记号处。![]()
4.探究评价:![]()
该探究实验在反应原理上就存在错误。我们都知道,反应物浓度越小,反应的速率越慢。当燃烧持续进行时,氧气的浓度越来越小,氧化的速率也越来越小。一旦燃烧放出的热量不足以维持可燃物在着火点以上温度时,燃烧便停止了。这也是有些物质不能在空气中燃烧,但能在氧气中燃烧的原因。因此,从这个意义上说,利用燃烧试图除尽空气中的氧气,是很难达到目的的。维持红磷燃烧需要的氧气浓度相对较高,因此就更无法除尽氧气了。很多教师在做该实验时,都发现,最终水面停在十分之一处,而不是五分之一处,原因就在于此。![]()
该实验装置可能发生气体泄漏的地方太多,加之燃烧的红磷伸入集气瓶中加热了内部的空气,使之外逸,都会导致实验的误差。![]()